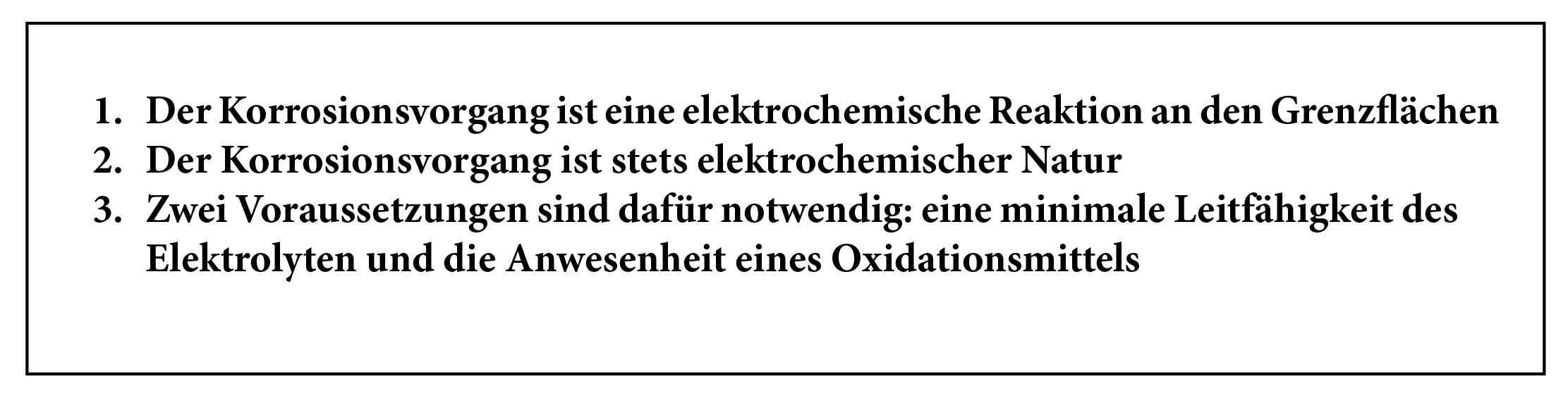
Wasserhärte und das Kalk-Kohlensäure-Gleichgewicht ist das heutige Thema. Aber noch einmal eine kurze Zusammenfassung der drei wichtigsten Erkenntnisse aus Folge 1 und 2 zu Korrosionserscheinungen:
Folge 3. Wasserhärte und das Kalk-Kohlensäure-Gleichgewicht
Wasserhärte und Kalkablagerungen
Die Wasserhärte dient im Wesentlichen zur allgemeinen Charakterisierung eines Wassers. Für die Beurteilung der Korrosivität ist sie nur von untergeordneter Bedeutung, da zwischen der Wasserhärte und dem Korrosionsvorgang kein unmittelbarer Zusammenhang besteht. Die Korrosivität eines Wassers kann im Gegensatz zur Wasserhärte nur im Zusammenhang mit einem bestimmten Werkstoff unter bestimmten Betriebsbedingungen abgeschätzt werden.
Diese kann nicht auf einfache Weise quantitativ beschrieben werden. Fälschlicherweise wird im Zusammenhang mit dem Kalk-Kohlensäure-Gleichgewicht immer wieder von aggressivem im Sinne von korrosivem Wasser gesprochen. Auch in vielen Prospekten von Wasserbehandlungsgeräten werden die Begriffe aggressives Wasser, Verkalkung, Inkrustierungen und Korrosion leider fälschlicherweise als Synonym verwandt.
Im Gegensatz dazu lässt sich die Wasserhärte relativ einfach berechnen. Die Kalkablagerung wird allein von den Bestandteilen des Wassers verursacht, vor allem durch die gelösten Calcium- und Hydrogenkarbonat- Ionen, die durch die sogenannte Karbonathärte charakterisiert werden. Die Gesamthärte setzt sich aus den Kationen von Calcium, Magnesium und den Anionen Sulfat und Karbonat zusammen.
Bei der Calciumkarbonatreaktion handelt es sich um eine Gleichgewichtsreaktion zwischen Kohlensäure, Kohlendioxid, Wasser und dem Calcium, die durch die Temperatur und den pH-Wert beeinflusst wird (Gleichungen 1+2). Das Ausmaß der Kalkabscheidung wird demnach durch zwei Faktoren verstärkt: Die Entfernung von gelöstem Kohlendioxid und/oder Erhöhung der Temperatur.
Mit zunehmender Temperatur wird daher der Prozess der Kalkablagerung beschleunigt. Schon deshalb sollen im Warmwasserbehälter die Temperaturen unter 60° C gefahren werden. Allerdings lässt sich diese Empfehlung aufgrund der Diskussion um das Legionella-Infektionsrisiko nicht mehr aufrecht halten. Der Kalk scheidet sich an der Stelle der Metall-wandung ab, die das Gleichgewicht der Reaktion nach rechts verschiebt.
Temperatur- und Druckerhöhungen wirken sich demnach stark auf das Kalk-/Kohlensäurengleichgewicht aus. Daher wird sich an der heißesten Stelle im Warm-wassersystem Kalk in Form von kristallinen Verbindungen (CaCO3) ausscheiden. Entscheidend ist also nicht die Wassertemperatur, sondern die Wandtemperatur an der Wärmeübertragungsfläche.
Die Reaktionsgleichung (1) an dieser Stelle zeigt wiederum, dass so dem Gleichgewicht ein Großteil des Kalks entzogen wurde, da CO2 entweicht und sich im restlichen Rohrsystem ein neues Gleichgewicht mit geringerem Calciumgehalt einstellen wird…